Une étude publiée dans Developmental Cell par l’équipe Kodjabachian dévoile comment les cellules multiciliées se distribuent à intervalles réguliers dans l’épiderme embryonnaire du xénope.
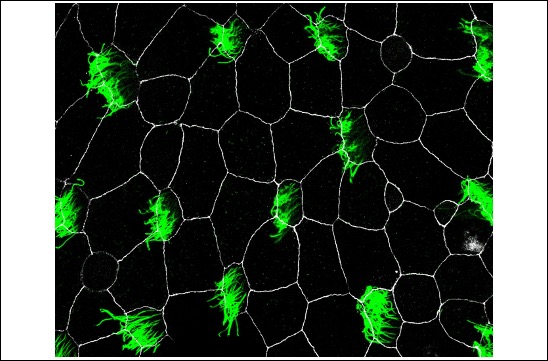
Chez le têtard de la grenouille xénope, comme chez d’autres animaux aquatiques, des milliers de cellules multiciliées s’insèrent à la surface de l’épiderme et agissent comme autant de balais mécaniques, grâce au battement coordonné et à haute fréquence de leurs cils. S’ensuit un courant puissant à la surface du têtard, qui chasse les micro-organismes environnants. Pour assurer une défense optimale, les cellules multiciliées se répartissent à intervalles réguliers. Comment diable font-elles ?
Les chercheurs ont observé que les cellules multiciliées naissent dans la couche interne de l’épiderme dans un patron désordonné. En quelques heures, la population entière se répartit de façon homogène, avant d’entamer son intercalation dans la couche de surface. En filmant ces cellules, ils ont constaté qu’elles projettent des extensions et se repoussent à chaque contact pour se tenir à distance. En parallèle, elles s’associent aux jonctions entre les cellules de la surface pour préparer leur intercalation. Les auteurs ont confirmé par modélisation mathématique que ces deux comportements sont suffisants pour conférer une distribution régulière à une population de cellules désordonnée.
Les scientifiques ont ensuite établi que le couple formé par le ligand Scf, produit par les cellules de surface, et le récepteur Kit, exprimé par les cellules multiciliées, est nécessaire et suffisant au déploiement de ces deux propriétés. La version membranaire du ligand Scf assure l’ancrage aux jonctions cellulaires, pendant que la version soluble, qui baigne le tissu épidermique, est nécessaire à la répulsion entre cellules multiciliées.
Digressons un peu ! Par temps de Covid, si on demande à un groupe d’individus de se répartir dans un espace clos, ils se déplaceront pour se séparer, typiquement à distance de bras tendus, ou en se servant de repères visibles, tels que des carreaux au sol, tout comme le font les cellules chargées de défendre le têtard contre les infections.
Il est fascinant de constater que l’auto-organisation des systèmes vivants, à l’échelle d’un groupe de cellules comme à celle d’un groupe d’individus, peut impliquer, face aux mêmes contraintes, des solutions simples et convergentes.
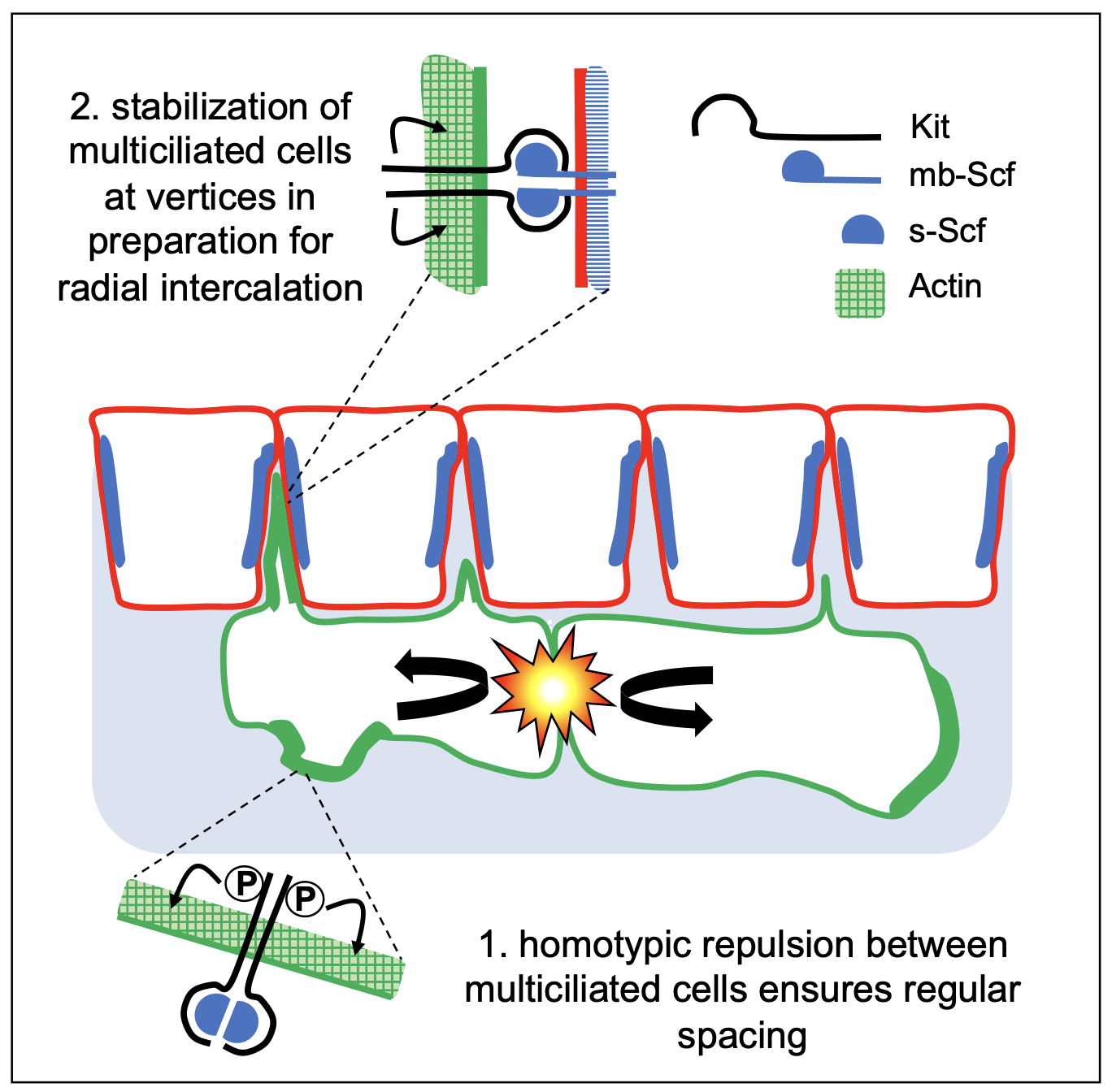
Copyright : Alexandre Chuyen, Andrea Pasini, Laurent Kodjabachian
En savoir plus:
The Scf/Kit pathway implements self-organised epithelial patterning.
Chuyen A, Rulquin C, Daian F, Thome V, Clement R, Kodjabachian L*, Pasini A*.
Developmental Cell
Contact
Laurent Kodjabachian – laurent.kodjabachian@univ-amu.fr
Andrea Pasini – andrea.pasini@univ-amu.fr